
MASSE ATOMICHE Difficoltà legate alla conoscenza della formula molecolare. Se l'acqua fosse HO avremmo la massa dell'ossigeno pari a 7,9367 g. Inizialmente. - ppt scaricare

Calcolo della formula minima (o “empirica”) di un composto a partire dalla percentuali in peso degli elementi che lo compongono Si ricava 1) il peso di. - ppt scaricare
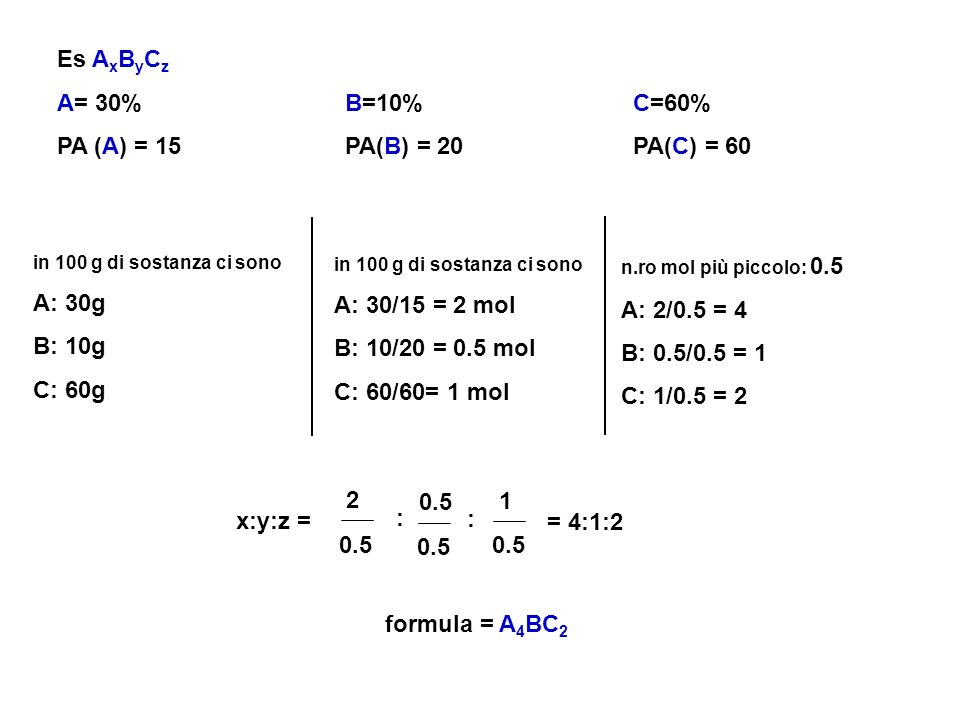
Calcolo della formula minima (o “empirica”) di un composto a partire dalla percentuali in peso degli elementi che lo compongono Si ricava 1) il peso di. - ppt scaricare

MASSE ATOMICHE Difficoltà legate alla conoscenza della formula molecolare. Se l'acqua fosse HO avremmo la massa dell'ossigeno pari a 7,9367 g. Inizialmente. - ppt scaricare

Calcolo della formula minima (o “empirica”) di un composto a partire dalla percentuali in peso degli elementi che lo compongono Si ricava 1) il peso di. - ppt scaricare

LAVOISIER Conservazione della massa nelle reazioni chimiche PROUST Un determinato composto contiene gli elementi in rapporti di peso indipendenti dal modo. - ppt scaricare














